
このページでは物質の状態変化とは何か。また、物質が状態変化する仕組みを簡単に図で解説しています。
1.物質の状態変化とは何か?
結論から言ってしまうと物質の状態変化とは、温度によって物質の状態(固体・液体・気体)が変化することを言います。
”固体・液体・気体の物質の3つの状態のこと”を「物質の三態」と呼びます。
上図のように物質には固体・液体・気体の3つの状態が存在していますが、それらの状態はその物質の温度によって変化します。
例えば水(液体)を0℃まで冷やすと氷(固体)に変化し、反対に水(液体)を熱して100℃(1気圧の場合)に達すると水蒸気(気体)に変化します。
このように物質は温度が変化することで、その状態も変化するんですね。
そして物質によって状態が変化する温度というのは異なります。
水(液体)は0℃で氷(固体)に、100℃で水蒸気(気体)に変化しますが、純アルコール(液体)は-114℃で固体に、78℃で気体に変化します。
なので一口に物質といっても、状態変化に必要な温度はそれぞれ異なるんですね。
このときに”物質が液体から固体に変化するときの温度”を「凝固点(ぎょうこてん)」、”液体から気体に変化するときの温度(正確には、液体が沸騰して気体に変化するときの温度)”を「沸点(ふってん)」と言います。
ちなみに一般的に知られている物質が状態変化する温度というのは、
あくまでも周囲の気圧の大きさが1気圧の場合によるものなので注意してください。
さて次の章で物質の状態変化の各名称について解説していきますね。
2.状態変化の各名称
物質の状態には固体・液体・気体の3つの状態(物質の三態)が存在しており、
物質が各状態へと変化する際にそれぞれ異なる名称が付けられています。
以前までは「気体→固体への状態変化=昇華」「固体→気体への状態変化=昇華」のようにどちらも同じ名称でしたが、2015年に日本化学会からの提案を受けて、最近の教科書では上図のように「気体→固体への状態変化=凝華(ぎょうか)」と記載されるようになっています。
簡単にまとめると下のようになります。
「気体→液体への状態変化=凝縮(ぎょうしゅく)」
「液体→気体への状態変化=蒸発(じょうはつ)」
「液体→固体への状態変化=凝固(ぎょうこ)」
「固体→液体への状態変化=融解(ゆうかい)」
「固体→(液体を経ずに)気体への状態変化=昇華(しょうか)」
「気体→(液体を経ずに)固体への状態変化=凝華(ぎょうか)」(以前までは「昇華」)
関連:凝結と結露の違いとは?
3.物質の状態が変化することで体積は変化するが、質量は変化しない
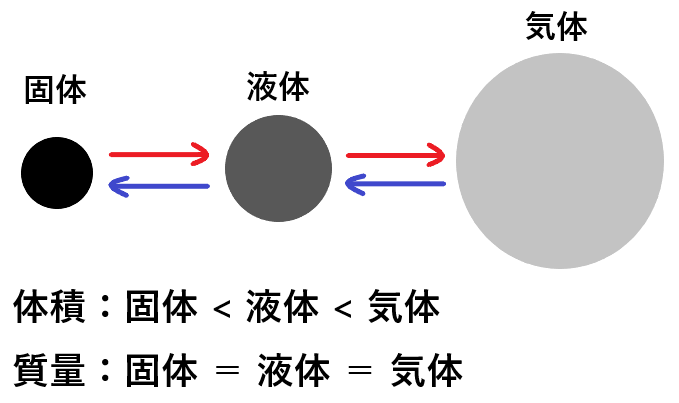
物質の状態が変化することでその物質の体積は変化していき、
ほとんどの物質は固体→液体→気体になるにつれて体積が大きくなります。
このときに物質の体積は変化しますが、質量については変化しないので覚えておきましょう。
(この法則のことを「質量保存の法則」と言います)
しかし、私たちがよく知っている物質で、上のような体積変化とは少し異なる物質があります。
その物質が何かというと、水になります。
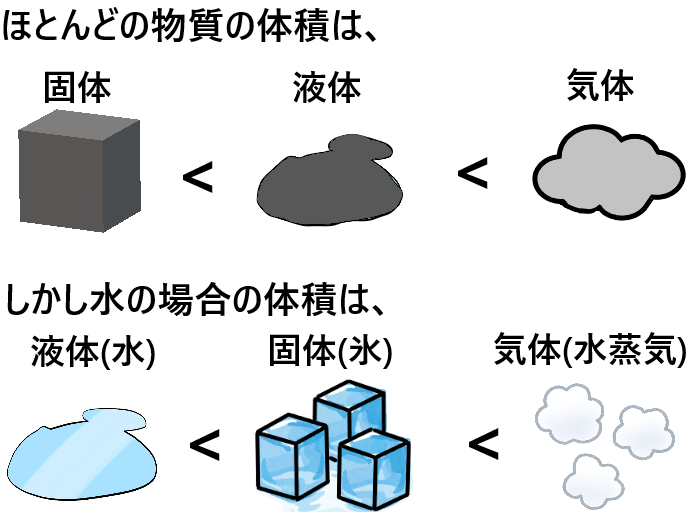
普通の物質であれば液体から固体に変化すると体積は小さくなりますが、
水に限っては氷(固体)に変化したときの方が体積が大きくなるんですね。
水(液体)の中に氷(固体)を入れると氷が浮くのは、氷の密度が水よりも小さいので氷が水の上に浮きます。
もし他の物質と同様に固体である氷が液体の水よりも体積が小さければ、
水の中に氷を入れても氷の方が水よりも密度が大きくなるために沈んでしまいます。
次の章で物質が状態変化する仕組みを簡単に図解していきますね。
4.物質が状態変化する仕組みを簡単に図解!
物質の状態には固体・液体・気体の3つの状態がありますが、
物質の状態はそれぞれ温度が変化することで異なる状態に変化します。
物質の温度が変化するというのは簡単にいうと、物質を構成している原子・分子の動きの速さが変化するということです。
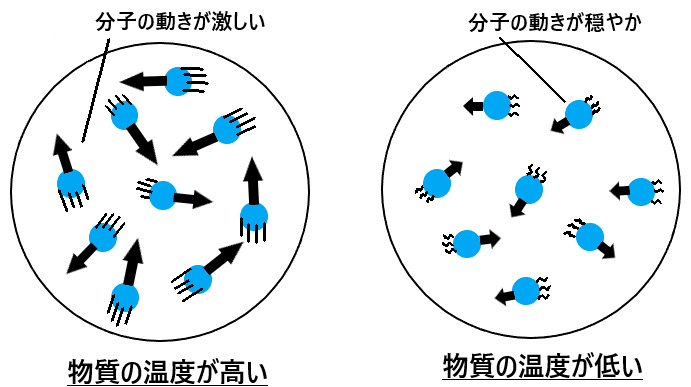
上図のように物質を構成している原子・分子の動きが速いほど温度は高く、反対に原子・分子の動きが遅いほどその物質の温度は低くなります。
(つまり熱というのは、”その物質を構成している原子・分子の動き(運動)のこと”を指します)
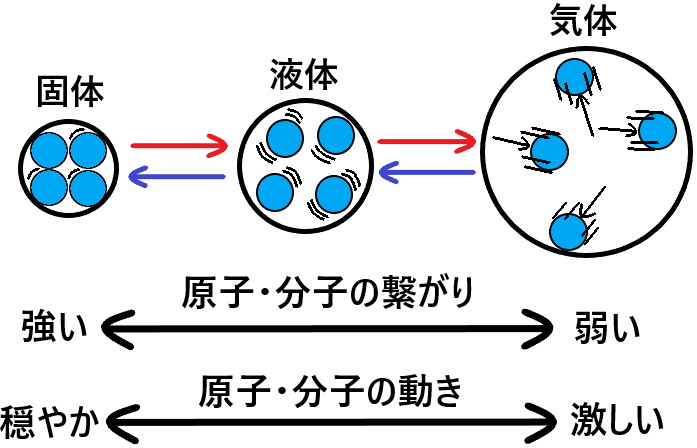
物質のそれぞれの状態(固体・液体・気体)というのは、
物質を構成している原子・分子同士による繋がり方で決まっています。
上図のように物質の原子・分子は、繋がり合うことでそれぞれの状態を形成しています。
(原子・分子同士には、お互いに引き合う力が働いており、それにより原子間・分子間での繋がりができます)
なので物質が状態変化する仕組みは、物質の温度が変化(原子・分子の動きの速さが変化)することで、その物質を構成している原子・分子の繋がり方が変わってしまうからなんですね。
物質の温度が高くなるほど原子・分子の動きが速くなるので繋がりが切れやすくなり、
反対に物質の温度が低くなると動きが遅くなるのでそれぞれが繋がりやすくなります。
(物質を構成している原子・分子の動きが速くなることで、原子間・分子間の引き合う力よりも大きくなり、繋がりが切れやすくなる)
だから物質は熱していくと原子・分子同士の繋がりがほとんど切れた状態の気体に変化し、冷やしていくと原子・分子同士の繋がりが強い固体に変化するんですね。
また物質が状態変化することで体積が変化しても質量が変化しないのは、
物質を構成している原子・分子の動きの速さが変わっただけだからです。
(体積が増えるのは、原子・分子同士の繋がりが切れることで自由に動ける範囲が増えるから)
なので上図のように、その物質を構成している原子・分子の数が増減しているわけではないため、物質が状態変化しても(体積は変化するが)質量は変わらない、というわけです。
(一般的な物質は上図のようになりますが水は例外で、水は4℃以下になると水分子が少し隙間をあけながら繋がり合うようになるため、氷(固体)の方が体積が大きくなります)
関連:熱と温度の違いとは?
以上が「状態変化とは何か?物質が状態変化する仕組みを簡単に図解!」でした。
5.まとめ
これまで説明したことをまとめますと、
- 物質の状態変化とは、”温度によって物質の状態(固体・液体・気体)が変化すること”。
- 状態変化する仕組みは、”物質の温度が変化(原子・分子の動きの速さが変化)することで、その物質を構成している原子・分子同士の繋がり方が変化するから”。
- 物質が状態変化しても(体積は変化するが)質量は変わらない。
関連ページ
<覚えておきたい知識>
鉄火巻きの具材は?、クリスマス・イヴはいつ?など
哀悼、重複、出生、集荷など
(写真あり)カラーボックス、ACアダプターなど
(写真あり)メンマ、かんぴょう、マシュマロなど
(地図あり)軍艦島、淡路島、屋久島など
<豆知識>
(写真あり)カレーの容器、視力検査の器具など
<名前は知っているけどわからないもの>
(写真あり)アヒージョ、マリトッツォなど
(写真あり)磯(いそ)、沿道、郊外など
(写真あり)うなじ、くるぶし、土踏まずなど
<よく使う言葉>
慣習、準拠、言わずもがな、明文化など
慣習的、致命的、便宜的、作為的など
互換性、慢性、普遍性、必然性など
蛙化、明文化、マンネリ化、擬人化など




